Formeln - Wärme (Energie, Kapazität, Avogadro)
Wärme im physikalischen Sinne ist über eine Systemgrenze hinweg
transportierte thermische Energie. Im allgemeinen Sprachgebrauch wird
der Begriff Wärme häufig mit der thermischen Energie selbst verwechselt.
Wärme
ist wie Arbeit an Transportvorgänge gebunden, daher eine Vorgangs- oder
Prozessgröße, im Gegensatz zu einer Zustandsgröße. Sie wird immer vom
wärmeren zum kälteren System transportiert, solange eine
Temperaturdifferenz zwischen zwei thermisch gekoppelten Systemen
besteht.
Wärme ist kein eigener Stoff, sondern eine Energieform, die
durch Prozesse (Reibung, Verbrennung, Bewegung) erzeugt wird. Erst
Mitte des 19. Jahrhunderts wurde allgemein akzeptiert, dass Wärme
Bewegung ist.
Wärmemenge und spezifische Wärmekapazität
Erwärmung oder Abkühlung eines Körpers ohne Änderung des Aggregatzustandes
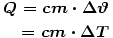
Bei Gasen ist zwischen cp und cv zu unterscheiden. Bei molaren Wärmekapazitäten gilt:
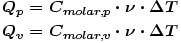
Bei einatomigen idealen Gasen gilt:
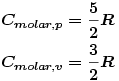
Bedeutung der Formelzeichen
Q zugeführte oder abgeführte Wärmemenge
(vatheta) Celsius-Temperatur
T absolute Temperatur
m Masse des Körpers
(nu) Stoffmenge des Gases
c spezifische Wärmekapazität des Stoffes
cp spezifische Wärmekapazität für das Gas (konstanter Druck)
cv spezifische Wärmekapazität für das Gas (konstantes Volumen)
Cmolar, p molare Wärmekapazität des Gases bei konstantem Druck
Cmolar, v molare Wärmekapazität des Gases bei konstantem Volumen
R universelle Gaskonstante
Erster Hauptsatz der Wärmelehre
Gesetz
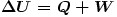
Sonderfall:
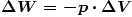
Bedeutung der Formelzeichen
(Delta)v Änderung der inneren Energie des Systems.
Q Wärmemenge, die von außen zugeführt wird, oder vom System abgegeben wird
W Arbeit, die von außen zugeführt wird, oder vom System abgegeben wird
(Delta)W Teilarbeit, die beid er Volumenänderung (Delta)V dem System
vom äußeren Druck p zugeführt wird oder die vom System gegen den
äußeren Druck p verrichtet wird